原发灶不明癌(CUP)是被诊断为转移性但原发灶不明的恶性肿瘤。CUP患病率约占所有癌症的4%,常表现为淋巴结、肺、肝脏、骨、脑、实体器官和腹膜或胸膜腔的转移。在CUP的IHC诊断中,虽然CK7和CK20组合常用于癌症评估的第一步,有4种表达模式(CK7+/CK20+,CK7+/CK20-,CK7-/CK20+,CK7-/CK20-),但要对CUP进行明确诊断还应得到器官特异性标志物的支持。这项回顾性调查旨在评估用于识别CUP的每个IHC标记的频率和准确性。
对2015 -2020 年Shahid Faghihi医院的所有资料完整的CUP患者进行回顾性分析和IHC研究(恶性黑色素瘤、肉瘤、生殖细胞瘤、神经内分泌癌和间皮瘤被排除在研究之外)。
收集到的595例CUP病例中,有307例符合参加本研究的条件,其中CUP最常见的表现部位是肝脏,但27%病例无法确定主要来源。转移病例原发器官的频率如图1。
图1. 转移癌原发器官的频率
结果显示,99.4%的CUP病例CK阳性,仅1例CK为阴性。对262例检测了 CK7/CK20的表达,评估其不同表达模式,如图2 。
图2. CK7/CK20在不同CUP临床诊断中的不同表达模式
CK7+/CK20-表达模式占所有CUP的55.3%,是最常见的模式。该模式常出现的原发灶分别为:不明来源(24.9%),肺(22.77%)、乳腺(17.24%)、胰胆系统(11.72%)、卵巢(6.9%)、甲状腺(4.13%)、子宫(3.44%)、上消化道(2.75%), 下消化道 (1.37%), 膀胱(1.37%), 前列腺(1.37%), 肝脏 (0.68%), 肾脏 (0.68%)和鳞状细胞癌(0.68%)。
这是当前研究中第二常见的模式,占所有CUP的19%。该模式常出现的原发灶分别为:前列腺 (28%)、不明来源(26%)、肾脏(14%)、肺(10%)、乳腺(8%)、上消化道 (4%)、肝脏 (4%)、鼻咽和鳞状细胞癌(6%) 。
CK7+/CK20+是第三常见模式,占所有CUP的15%。该模式常出现的原发灶分别为:不明来源(38.5%)、胰胆系统(23.07%)、上消化道(10.25%)、下消化道(7.69%)、膀胱(10.25%)、肺(5.12%)和卵巢(5.12%)。
CK7-/CK20+模式最不常见,占所有CUP的10.7%。该模式常见的原发灶分别为:下消化道(60.73%)、不明来源(21.42%)、阑尾(7.14%)、上消化道(7.14%)和膀胱(3.57%)。表1和表2为CK7/CK 20不同模式和器官特异性IHC标志物频率。表1. CK7/CK20不同表达模式在不同原发器官的频率分布
表2.器官特异性IHC标志物在不同临床诊断中的频率分布
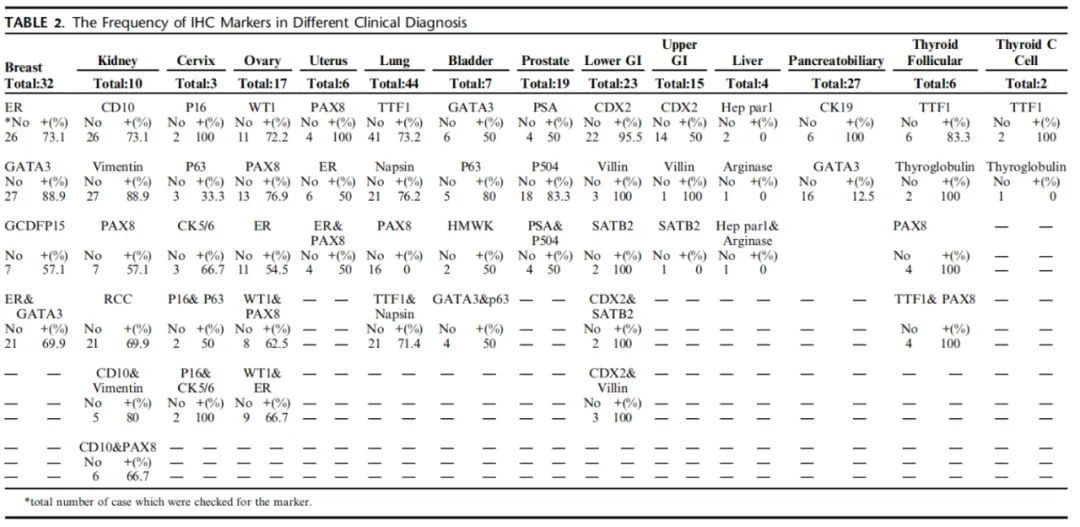
图3-6是基于CK7/CK20染色模式和器官特异性标志物对肿瘤原发灶鉴定的一些示例:

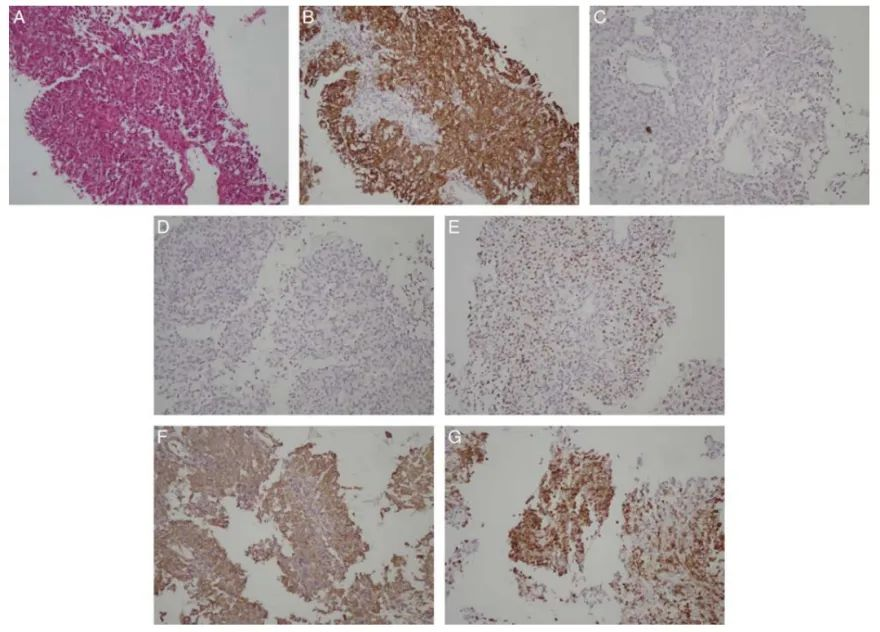
图3.下消化道起源的转移癌(A,HE 400×;B-E,CK7、CK 20、CDX2和SATB2的IHC染色结果:CK7-/CK20+,CDX2+,SATB2+)。
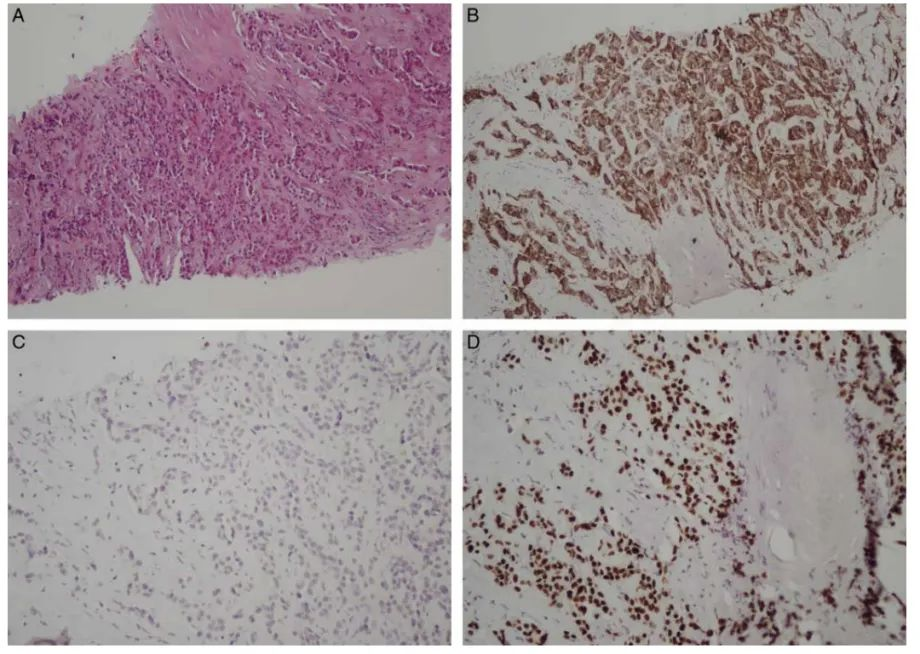
图4. 乳腺起源的转移癌(A,HE 250×;B-D: CK7、CK20 和 GATA3的IHC染色结果:CK7+/CK20-,GATA3+)。图5. 肾脏起源的转移癌(A,HE 400×;B-G:CK、CK7、CK20、Pax-8、波形蛋白和CD10的IHC染色结果:CK7-/CK20-)。图6. 胰胆起源的转移癌(A,HE 250×;B-E:CK7、CK20、CK19和CDX2的IHC染色结果:CK7+/CK20+,CK19+,CDX2-)。
胃肠道起源的病例检测到了所有的CK7/CK20表达模式。研究显示,CDX2在95.5%下消化道和50%上消化道起源病例中阳性表达,并在超90%结直肠癌中阳性表达,但它不是下消化道起源转移癌的良好预测标志物,因为它可能在所有胃肠道起源的转移癌中都呈阳性表达,在胃癌中的阳性率为18%-70%以上,在74%胃起源转移到卵巢的病例中呈阳性表达。本研究中,SATB2在下消化道起源的CUP中阳性表达,对结直肠起源的转移癌有高敏感性和特异性。Ma等人证明了SATB2是一种新标志物,在85%的结直肠原发性和转移性印戒细胞癌阳性表达,但它不适合作为上消化道起源的转移癌标志物。本研究中,Villin在上、下消化道起源的转移癌中阳性表达。研究显示,Villin在结直肠癌中的阳性率很高:75%-90%以上,特别是分化良好的病例。另外,Villin表达不局限于胃肠道癌,在40%胰腺癌、78%食道癌和64%黏液性卵巢癌中也呈阳性表达。CDX2、Villin和SATB2有助于识别下消化道起源的转移癌。对可能是上消化道来源的病例,Villin和CDX2联合使用可提高诊断率。4例临床诊断为肝脏起源的转移癌,但未经准确的病理诊断。CK表达模式分别为CK7-/CK20-(66.7%)和CK7+/CK20-(33.3%),但Hepatocyte和Arginase-1均为阴性。研究表明,Hepatocyte 在70%-100%肝癌中阳性表达,敏感性和特异性为70%和84%,Arginase-1对肝癌的敏感性为 96%,即使在低分化肝细胞癌中也是如此。但这4例并不表达Hepatocyte和Arginase-1,应归类为未确定来源。86.2%和13.8%的乳腺源病例分别出现CK7+/CK20-和CK7-/CK20-表达模式。ER、GATA3、GCDFP-15在乳腺源病例中的阳性表达率分别为73.1%、88.9%和57.1%。研究显示,GATA3对乳腺癌诊断的敏感性高于GCDFP-15,故ER和GATA3联合使用有助于诊断大部分乳腺癌。 CK7-/CK20-是肾脏起源的转移癌最普遍的表达模式,其次是CK7+/CK20-。CD10、Vimentin和 Pax-8在超70%的肾癌中阳性表达,可确定肾脏起源。研究表明,Pax-8在转移性癌中的阳性率更高,是原发和转移性肾癌的特异标志物;CD10在91%肾透明细胞癌中阳性表达,Vimentin对肾透明细胞癌的敏感性为100%。本研究显示:Vimentin、Pax-8和CD10的联合应用,有助于鉴定肾脏起源的转移癌。宫颈起源的转移癌普遍表达CK7+/CK20-模式。所有评估病例均分化不良,不能通过组织形态学确定宫颈癌的类型(即鳞癌和腺癌),因此,使用p16、p63和CK5/6 的IHC套餐诊断宫颈癌。据报道,它们对诊断宫颈鳞癌有良好的敏感性和特异性,Wang等人发现p16在转移至肺的宫颈鳞癌中阳性表达率为98%。83.3%卵巢起源的转移癌表达模式为CK7+/CK20-,其余为CK7+/CK20+。CK7+/CK20-病例中,72.7% WT1阳性,6.9% Pax-8阳性,54.5% ER阳性。研究发现,在卵巢起源的转移癌中,WT1阳性率超90%,Pax-8和ER的阳性率分别为70%-99%,85%-90%。本研究显示:66.7%卵巢起源的转移癌同时表达WT1和Pax-8。由于卵巢浆液性癌是最具高转移风险的常见卵巢上皮肿瘤,因此,WT1、Pax-8和ER可作为诊断卵巢起源的转移癌(尤其CK7+/ CK20-模式)的高敏感IHC套餐。诊断 CK7+/CK20+模式CUP时,应考虑黏液癌,CDX2等标志物可能有用。所有子宫起源的转移癌均表达CK7+/CK20-模式。Pax-8和ER分别在100% 和50%的病例中阳性表达。研究表明84%-93%子宫内膜癌Pax-8阳性表达,因此,Pax-8是确定子宫起源的宫外部位腺癌的有用标志物。此外,Alkushi和 Kounelis 等人分别发现ER在 73% 和 54% 子宫内膜癌中阳性表达。82.5%肺起源的转移癌表达CK7+/CK20-模式,12.5%表达CK7-/CK20-模式,5%表达CK7+/CK20+模式。TTF-1在73.2%病例中阳性表达,这与之前的研究一致,TTF-1 在各种肺癌中的阳性表达率为70%-100%,但低分化腺癌TTF-1 阳性表达率较低。76.2% 肺起源的转移癌Napsin A阳性表达。研究表明,Napsin A 在超80%患者中阳性表达,在诊断肺起源的转移癌方面比TTF-1更敏感。Pax-8在所有肺起源的转移癌中阴性,有助于将肺起源和甲状腺起源的肿瘤区分开,因为这两种癌TTF-1均阳性。研究表明,TTF-1 和 Napsin A 联合使用对检测肺腺癌有较高的敏感性。所有甲状腺起源的转移癌均表达CK7+/CK20-模式。6例甲状腺滤泡细胞起源的病例TTF-1阳性率为83.3%,Thyroglobulin和Pax-8阳性率均为100%。2例髓样癌TTF-1、Calcitonin阳性,Thyroglobulin阴性,这与之前的研究一致:TTF-1 和 Pax-8在甲状腺起源的转移癌均显示出高敏感性。与甲状腺髓样癌和未分化癌相比,这些标志物的阳性表达更常见于分化良好的甲状腺滤泡起源转移癌(乳头状癌和滤泡状癌)。另一方面,Zhang 等人发现与之前的研究不一致:Pax-8 在31.2% 乳头状癌和 40% 滤泡癌中阳性表达。Thyroglobulin阳性表达率在甲状腺滤泡上皮癌和转移部位间存在差异:60%-100% 不等。TTF-1、Thyroglobulin、Pax-8作为IHC套餐,对滤泡细胞起源的癌有100%的敏感性。Thyroglobulin、TTF1 和Calcitonin作为IHC套餐,对C细胞起源的癌有很高的预测性。87.5%前列腺起源的转移癌表达CK7-/CK20-模式 ,其余为CK7-/CK20+。AMACR/p504s 和PSA分别在83.3%和50%病例中阳性表达。50%病例可观察到 PSA 和 AMACR/p504s 共表达。研究表明,PSA在前列腺癌中表达有很高的敏感性和特异性,但其在转移部位应用较少,与高级别前列腺癌相比,高分化前列腺癌的 PSA 阳性率更高。AMACR/p504s在80%-100%前列腺癌阳性表达,有较高的敏感性。65.4%胰胆起源的转移癌表达CK7+/CK20-模式,其余表达CK7 +/CK20+,所有患者CK19均阳性表达,12.5%患者GATA3阳性表达。研究表明,CK19 在 100% 肝脏转移性胰腺腺癌中阳性表达,在胰腺癌诊断中有100% 敏感性。胰腺导管癌是 GATA3 阳性表达率最高的非乳腺癌之一的病种,敏感性为 37%。Clark 等人的研究显示,10% 胰腺癌GATA3阳性表达。尽管没有可检测胰胆管癌的特异性标志物,但CK19可能有助于诊断胰胆系统起源的病例。应注意的是,细胞质 IHC 标志物的表达常受肿瘤分化程度影响。许多情况下,肿瘤细胞分化和组织特异性定位于胞质的标志物易在转移中丢失,而定位于细核的标志物受影响最小。本研究中,与源自子宫颈、胰胆系统和肝脏的癌相比, IHC 更容易检测到源自上下消化道、乳房、肾脏、前列腺、卵巢、肺和甲状腺的癌。抗体名称 | 产品编号 | 克隆号 | 细胞定位 |
CK7 | MAB-0828 | MX053 | 胞质 |
CK20 | MAB-0834 | MX059 | 胞质 |
CDX2 | RMA-0631 | EPR2764Y | 胞核 |
SATB2 | RMA-0750 | EP281 | 胞核 |
Villin | MAB-0540 | CWWB1 | 胞质 |
Hepatocyte | MAB-1034 | MX119 | 胞质 |
Arginase-1 | RMA-0806 | EP261 | 胞质/胞核 |
GATA3 | RMA-1067 | EP368 | 胞核 |
GCDFP-15 | MAB-1035 | MX120 | 胞质 |
ER | Kit-0012 | SP1 | 胞核 |
CD10 | MAB-0668 | MX002 | 胞质/胞膜 |
Vimentin | MAB-0735 | MX034 | 胞质 |
Pax-8 | RMA-1024 | MXR013 | 胞核 |
p63 | MAB-0694 | MX013 | 胞核 |
CK5/6 | MAB-0744 | MX040 | 胞质 |
WT-1 | MAB-0678 | MX012 | 胞核 |
TTF-1 | MAB-0677 | MX011 | 胞核 |
NapsinA | MAB-0704 | MX015 | 胞质 |
Thyroglobulin | MAB-0797 | 2H11+6E1 | 胞质 |
Calcitonin | RMA-0553 | SP17 | 胞质 |
AMACR/p504s | RMA-1023 | MXR012 | 胞质 |
PSA | MAB-0719 | MX030 | 胞质 |
CK19 | MAB-0829 | MX054 | 胞质 |
参考文献:
[1] Mokhtari Maral,Safavi Dornaz,Soleimani Neda, et al. Carcinoma of Unknown Primary Origin: Application of Immunohistochemistry With Emphasis to Different Cytokeratin 7 and 20 Staining Patterns[J]. Applied Immunohistochemistry & Molecular Morphology,2022.
更多信息,请详询:800-8581156 或 400-889-9853